Zwavelzuur ook bekend als H2SO4, is een van de meest gebruikte chemicaliën ter wereld. Het wordt gezien als een van de belangrijkste chemicaliën van de wereld. Het wordt veel gebruikt en heeft vele toepassingen, zoals in fabrieken en in laboratoria.
In deze blog kijken we naar de belangrijkste eigenschappen van zwavelzuur.
Moleculaire Structuur en Chemische Formule van Zwavelzuur
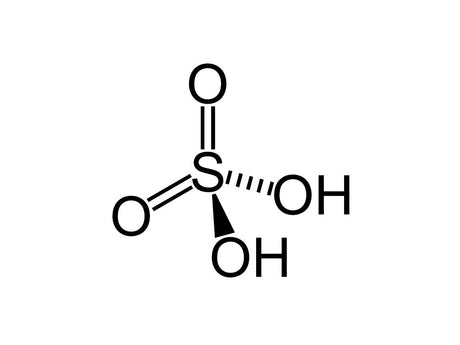
Zwavelzuur heeft de chemische formule H2SO4. Het bestaat uit twee waterstofatomen (H), één zwavelatoom (S) en vier zuurstofatomen (O).
De molecuulstructuur bestaat uit een zwavelatoom in het midden, dat verbonden is met vier zuurstofatomen. Twee van deze zuurstofatomen zijn dubbel gebonden, en twee zijn enkel gebonden. Door deze structuur is zwavelzuur zo'n sterk zuur en heeft het sterke oxiderende eigenschappen.
Fysische Eigenschappen: Dichtheid, Viscositeit en Kookpunt
Zwavelzuur is een kleurloze, dikke vloeistof met een hoge dichtheid van ongeveer 1,84 g/cm3 (bij 98% concentratie). Het kookt bij ongeveer 337°C, maar begint bij lagere temperaturen al uit elkaar te vallen. Het is ook heel stroperig, hierdoor vloeit het langzaam. Zwavelzuur is dikker dan water.
Zuurgraad en Corrosieve Eigenschappen
Zwavelzuur is een heel sterk zuur met een pH-waarde die lager is dan 1, afhankelijk van de concentratie. Het is erg bijtend en kan ernstige schade veroorzaken aan de huid en andere materialen. Daarom moet je altijd beschermende kleding en handschoenen dragen als je met zwavelzuur werkt.
Reacties met Metalen en Andere Stoffen
Zwavelzuur reageert heel sterk met veel metalen, waarbij vaak waterstofgas vrijkomt. Waterstofgas is erg ontvlambaar en kan ontploffen als het in aanraking komt met een vonk of warmte. Dit maakt het werken met zwavelzuur extra gevaarlijk.
Een voorbeeld hiervan is de reactie met zink. Als zink met zwavelzuur reageert, ontstaat zinksulfaat en komt er waterstofgas vrij. Zwavelzuur kan ook reageren met oxiden en hydroxiden om zouten te vormen. Dit is belangrijk voor veel industriële toepassingen.
Concentraties en Verdunningen
Zwavelzuur is verkrijgbaar in verschillende concentraties, van geconcentreerd (98%) tot verdund. Geconcentreerd zwavelzuur wordt veel gebruikt in fabrieken, terwijl verdund zwavelzuur vaak wordt gebruikt in laboratoria en op scholen. Als je zwavelzuur verdunt, moet je altijd heel voorzichtig zijn: voeg altijd langzaam het zuur aan water toe en nooit andersom. Dit voorkomt gevaarlijke spatten.
Thermische Stabiliteit en Ontleding bij Hoge Temperaturen
Als zwavelzuur verhit wordt, begint het uit elkaar te vallen. Hierbij komen zwaveldioxide (SO2), waterdamp en zuurstof vrij. Deze ontleding kan gevaarlijk zijn, vooral in afgesloten ruimtes. Ondanks deze ontleding blijft zwavelzuur stabiel genoeg om te gebruiken in processen waarbij verhitting nodig is, als je het goed onder controle houdt.
Oplosbaarheid en Interactie met Water
Zwavelzuur lost heel goed op in water en dit proces komt met veel warmte vrij. Dit kan gevaarlijk zijn als het niet goed gebeurt. Daarom moet je altijd zuur aan water toevoegen, en niet andersom, om spatten en brandwonden te voorkomen.
Oxiderende en Dehydraterende Eigenschappen
Zwavelzuur heeft sterke oxiderende eigenschappen, vooral als het geconcentreerd is. Het kan organische stoffen oxideren en werkt ook als een dehydratiemiddel, wat betekent dat het water uit materialen haalt. Dit zie je duidelijk als je zwavelzuur aan suiker toevoegt: het zuur haalt het water uit de suiker, waardoor een zwarte, koolachtige massa overblijft.
Conclusie
Zwavelzuur is een interessante stof met krachtige eigenschappen. Van de moleculaire structuur tot de reacties met andere stoffen, zwavelzuur speelt een belangrijke rol in zowel industriële processen als laboratoriumexperimenten. Maar het is ook een van de gevaarlijkste chemicaliën, dus voorzichtigheid is altijd nodig. Het begrijpen van de eigenschappen van zwavelzuur is belangrijk voor veilig gebruik en effectieve toepassingen.